研究概要【がんワクチン分子部門】
部門長:山田 亮
2011年度は我々にとって節目の年でした。これまで3期15年間続いた文部科学省の私立大学高度化推進事業(ハイテクリサーチセンター整備事業)が終了し、私立大学戦略的研究基盤形成支援事業のもとに新たな5年間のスタートを切ることができました。また、前立腺がんを対象とするテーラーメイドがんペプチドワクチンの開発が科学技術振興機構(JST)の研究成果最適展開支援プログラム(A-STEP)に採択され、富士フイルム(株)と共同で医薬品承認に向けての今後の開発を行うこととなりました。
テーラーメイドペプチドワクチンの臨床試験は橋渡し臨床研究と薬事承認のための治験の2本立てで進められていますが、本年度は脳腫瘍を対象として薬事承認のための最終段階である第Ⅲ相治験を医師主導治験として開始しました。橋渡し臨床研究ではがん患者における免疫抑制状態の解除を目的としたシクロフォスファミドや漢方薬との併用療法のランダム化比較試験もすすめられ、平成21年4月に開設したがんワクチン外来も順調に受診者数を伸ばしています。
また、テーラーメイドペプチドワクチンの煩雑性を解消するための次世代型がんペプチドワクチンであるカクテル製剤の第Ⅰ相治験を医師主導治験として開始しました。
Cancer Vaccine Development Division
Research overview
The year 2011 was a big year for our division. Fiscal 2010 was the last year of our third 5-year term (total 15 years) of support under the program for the establishment of high-tech research centers at private universities, sponsored by the Ministry of Education, Culture, Sports, Science and Technology (MEXT), Japan. From 2011, our research activities are continuing under the support of a new 5-year research grant from MEXT, under its Private University Strategic Research Foundation Support Program. We have also obtained a new grant from the Japan Science and Technology Agency (JST) for development of personalized peptide vaccines for prostate cancer patients, under its “Adaptable and seamless technology transfer program through target-driven R&D (A-STEP)” program. This project is being promoted in collaboration with Fuji Film Corporation.
Two types of clinical studies involving personalized peptide vaccines are currently ongoing, i.e., translational research, and IND (investigational new drug application) clinical research. An investigator-initiated phase III IND clinical trial, the last stage of NDA (new drug application), of a personalized peptide vaccine for advanced glioblastomas is now underway. Translational research on combination therapies of personalized peptide vaccination with cyclophosphamide or traditional Chinese herbal medicines, both of which are used to improve immune suppression in cancer patients, have also been started as randomized trials. The total number of patient visits and the number of new patients at the cancer vaccine outpatient clinic (established in April of 2009) are both gradually increasing. An investigator-initiated clinical trial of a cocktail peptide vaccine, a next generation cancer vaccine designed to simplify some of the more complicated steps in the process, such as HLA-typing and immune tests, has also been started under an IND.
Akira Yamada,Ph.D.,Division Chief
研究活動
腫瘍関連抗原由来のCTLエピトープに対する液性免疫応答
がん免疫療法は外科療法、化学療法、放射線療法に続くがんの第四の治療法として最近特に注目を浴びている。現在久留米大学では、がん免疫療法の一つとしてペプチドワクチン療法の臨床試験を実施しており、免疫モニタリング法の一つとして、ワクチンに使用している腫瘍関連抗原由来ペプチドに対する特異的抗体の測定を行っている。これまでの検討では、がんペプチドワクチン投与前・投与後に抗ペプチド抗体が高いがん患者ではワクチン投与後の生命予後が延長することが見出されているが、健常人またはがんペプチドワクチン非投与がん患者における抗ペプチド抗体に関しては明らかにされていない。そこで、健常人またはがんペプチドワクチン非投与がん患者における抗ペプチド抗体の測定を試みた。
CTLエピトープに対する抗体は健常人血漿/血清中においても検出可能である
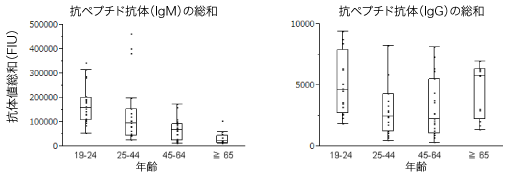
CTLエピトープに対する抗体(IgM)は加齢とともに減少する傾向にあることが示唆された。また、IgGは64歳までは減少するが、65歳以上で上昇することが見出された。
ペプチドワクチン非投与がん患者血漿/血清中のCTLエピトープに対するIgG1の総和は生命予後と相関する
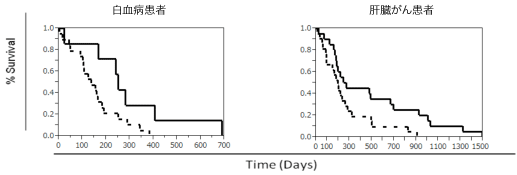
がんペプチドワクチン非投与がん患者での抗ペプチド抗体の総和が高い群(実線)と低い群(破線)において、ログランクテストを行った。がんペプチドワクチン非投与がん患者において、抗ペプチド抗体総和が高い群において生命予後の延長が示唆された。
以上の結果から、がんペプチドワクチン療法に使用されているCTLエピトープペプチドに対する液性免疫応答は健常人においても検出可能であることが示唆された。また、がんペプチドワクチン非投与がん患者において、抗ペプチド抗体と生存期間と有意に相関することが判明した。
Humoral immune responses to CTL epitope peptides from tumor-associated antigens are detectable in humans
Since the discovery of epitope peptides derived from human tumor-associated antigens (TAA) that are capable of inducing cytotoxic T lymphocyte (CTL) responses, peptide-based cancer vaccination has been extensively studied as a potentially attractive cancer treatment. However, the clinical benefits of this treatment modality have been limited, and there are several hurdles to overcome for further development. One of them could be a better understanding of the roles of humoral responses against TAA. We previously reported that IgG levels to TAA-derived CTL epitopes were well correlated with overall survival (OS) in advanced cancer patients who received personalized peptide vaccination. These results suggested that humoral responses against CTL epitope peptides might play an important role in protection from cancer progression. However, the prevalence and/or clinical significance of immunoglobulins (Igs) to TAA-derived CTL epitope peptides remain to be investigated in healthy donors (HD) and non-vaccinated cancer patients. Our results demonstrated that Ig responses to CTL peptides derived from TAA were widely detectable in humans, and anti-peptide IgG1 levels correlated with OS in cancer patients. Measurement of Igs specific to CTL peptide could be a potential prognostic factor for OS of patients with malignant diseases.
テーラメイドがんペプチドワクチン療法における血液バイオマーカーの同定
テーラメイドがんペプチドワクチン療法により治療された標準治療抵抗性の進行性非小細胞肺がんおよび胆道がん患者よりワクチン投与前後に採取した血液サンプル(末梢血単核球及び血漿)を用いて、臨床効果と相関性を示す血液バイオマーカーの同定を試みた。
肺がん
テーラメイドがんペプチドワクチン療法により治療された進行性非小細胞肺がん患者41例よりワクチン投与前後に採取した血液サンプルの解析データおよび臨床所見を用いて多変量Cox回帰解析を行った。ワクチン投与前の因子のなかではCRP低値が有意に全生存期間の延長に相関した(添付図参照)。また、ワクチン投与後の因子では、CRP低値、CD3⁺CD26⁺細胞の上昇が有意に全生存期間の延長に相関した(Yoshiyama K, et al., Int J Oncol, 40: 1492-1500, 2012)。
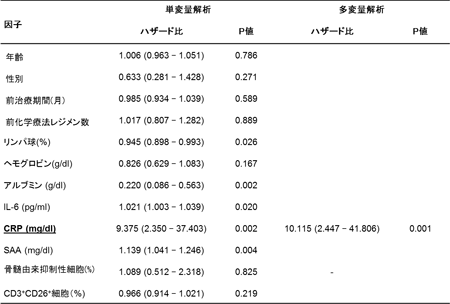
胆道がん
テーラメイドがんペプチドワクチン療法により治療された進行性胆道がん患者25例よりワクチン投与前後に採取した血液サンプルの解析データおよび臨床所見を用いて多変量Cox回帰解析を行った。ワクチン投与前のインターロイキン6(IL-6)低値、アルブミン高値、選択されたペプチド数が有意に全生存期間の延長に相関した(添付図参照)。ワクチン投与後の因子においてはIL-6低値、投与されたペプチド数が有意に全生存期間の延長に相関した(Yoshitomi M, et al., Exp Ther Med, 3: 463-469, 2012)。
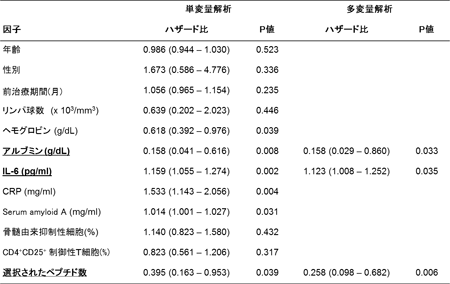
以上の結果から、テーラメイドがんペプチドワクチン療法により治療された進行がん患者においては治療前の血漿中のCRP、IL-6などの炎症性因子、栄養状態、および、選択されたペプチド数が全生存期間と有意に相関することが判明した。現在、これらの研究成果をもとに、進行性がん患者における炎症反応を防ぐ目的でヒト化抗ヒトIL-6レセプター抗体(トシリズマブ)や漢方薬(十全大補湯、大建中湯)を併用したテーラメイドがんペプチドワクチン療法の有効性を検討する臨床試験を開始している。
Identification of Predictive Biomarkers in Cancer Patients Receiving Personalized Peptide Vaccination
We have previously demonstrated the feasibility of our novel immunotherapeutic approach, personalized peptide vaccination (PPV), in which vaccine antigens are selected and administered on the basis of the pre-existing host immunity before vaccination. However, it is critical to identify reliable biomarkers for selecting patients who would most likely benefit from PPV, since only a subset of patients show clinical responses to this treatment. In order to further improve the clinical efficacy of PPV, we tried to identify pre-vaccination biomarkers for predicting prognosis in advanced cancer patients receiving PPV. In non-small cell lung cancer patients receiving PPV (n=41), multivariate Cox regression analysis showed that lower CRP level before vaccination was a significantly favorable factor for overall survival (OS). In biliary tract cancer (n=25), lower IL-6 and higher albumin levels before vaccination and greater numbers of peptides selected for vaccination were significantly favorable factors for OS in the vaccinated patients. Taken together, these findings suggested that less inflammation, better nutrition, and pre-existing immune responses to greater numbers of antigens before vaccination may contribute to better responses to PPV. Evaluation of inflammatory and nutritional status and pre-existing host immunity to antigens before vaccination could thus be useful in selecting cancer patients who would benefit from PPV. Our findings might provide new insights for designing and improving cancer vaccines.
テーラーメイドペプチドワクチン臨床試験における末梢血単核球を用いた遺伝子発現解析
これまでのテーラーメイドペプチドワクチン臨床試験において、長期生存群と短期生存群の臨床的背景をワクチン投与前において比較すると、ほとんどの場合において有意な差が認められないことが多い。がんワクチンをより有効な治療法としていくためにはワクチン投与前もしくはワクチン投与後早期の臨床効果の予測が可能なバイオマーカーの探索が重要であると考えられる。
当研究グループではがん患者末梢血単核細胞に着目し、その遺伝子発現解析により生存期間と関連する遺伝子があるか探索している。前立腺がんをモデルケースとしてこれまでの臨床試験検体より遺伝子発現解析を実施し、これまでに長期生存群(900日以上生存)と短期生存群(300日未満生存)の比較において、両群で発現に差が認められる遺伝子群を見いだしている(Komatsu N et.al. Gene expression profiles in peripheral blood as a biomarker in cancer patients receiving peptide vaccination. Cancer. 2012)。
しかしながら実際の臨床試験に参加の患者の多くは中間生存群(300日以上900日未満生存)に当てはまるため、遺伝子発現解析によるがんワクチン感受性診断への応用のためには、生存期間と関連する遺伝子の探索は中間生存群も考慮することが重要であると考えられる。そこで中間生存群を含めた遺伝子発現解析を実施した。
生存期間と遺伝子発現についてコックス・ハザード解析などを実施し、9の遺伝子について有意に相関を認め、そのうち長期生存群と短期生存群のみで解析したものとの重複も一部認められた。
がんワクチン感受性診断への実用化に向けて、見いだした遺伝子群を中心として今後も検証を重ねていくことが必要である。
Gene expression analysis in PBMC of cancer patients enrolled in personalized peptide vaccine trials
We analyzed gene expression profiles in peripheral blood mononuclear cell(PBMC)obtained from two groups of advanced castration-resistant prostate cancer patients, those who survived for > 900 days and those who died < 300 days after treatment with personalized peptide vaccine. Some genes were differentially expressed between the two groups, but it is still unclear whether these genes are correlated with overall survival either in typical survival cases or in the advanced prostate cancer patients who enrolled in personalized peptide vaccine trial.
Gene expression studies in pre-vaccination PBMCs were performed by Illumina® bead arrays, and were analyzed with the use of SAS statistical software(version 9.2, SAS Institute).
The hazard ratios for the comparison between overall survival from the date of first vaccine administration and gene expression levels were estimated by Cox model. After multiple testing correction using the Bonferroni adjustment, nine genes had an adjusted P -value less than 0.05. Some of these genes were found only in the group that survived for > 900 days, others were unique to the group who died < 300 days after treatment, and some genes were present in both groups. We are continuing to study these 9 genes to determine their usefulness as biomarkers in evaluating potential patient response to cancer vaccines.
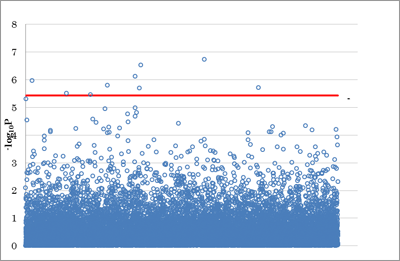
図)遺伝子発現と生存期間の関連性についてのマンハッタンプロット
ひとつの青いマルは一つの遺伝子発現と生存期間との関連性の有意水準を表す。赤いラインよりも上部にプロットされている遺伝子が生存期間と関連する遺伝子。
進行脳腫瘍に対するテーラーメイドがんペプチドワクチン実用化研究の進捗
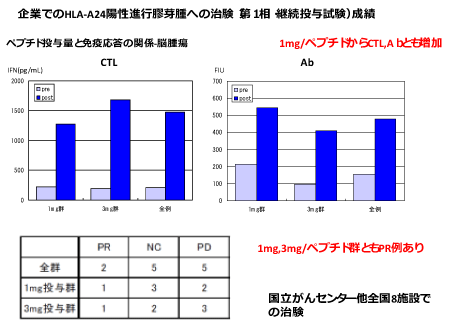
1.第1相・第2相臨床試験:2005年10月よりHLA-A24陽性膠芽腫患者に対してITK-1単独投与による第Ⅰ相臨床試験、および2006年1月よりHLA-A24陽性エストラムスチン不応答性再燃前立腺がん症例を対象としてITK-1・低用量エストラムスチン併用投与による第Ⅰ相臨床試験を開始した。何れの試験も1mg、3mgおよび5mg投与群各6例に対して各被験者のペプチドに対する抗体価に応じた4種類のペプチドを選択し、毎週6回皮下投与して安全性を検討した。また、引き続き好ましい経過が得られている被験者に対して、最長2年間の継続投与試験も実施した。その結果、安全性に関して、因果関係が否定できない主な有害事象は投与部位の反応であり、そのうちCTCAEグレード3の症例を1例認めたが、それ以外はいずれもCTCAEグレード2以下の軽度のものであった。有効性に関して、MSTは10.6ヶ月であった。本治験では、現在、標準治療とされているテモゾロミド治療後の被験者が12例中10例含まれており、標準治療後の患者に対して、さらなる延命効果が示唆された。また、MRIによる画像診断では、2方向測定法において12例中2例に奏効例が認められ、無増悪生存期間の中央値は、3.1ヶ月であった。(詳細は参考論文参照)
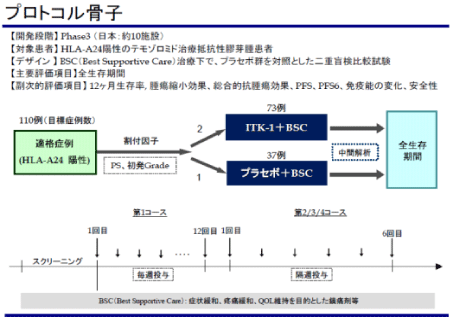
2.第3相臨床試験:PMDA対面助言:当該研究であるペプチドワクチンの第Ⅲ相臨床研究を開始するにあたり、ITK-1第Ⅱ相試験終了後相談をPMDAの第5部新薬審査部に対して実施し、治験実施計画書骨子を完成させた(下図)。また厚生労働省のがん研究支援事業や久留米大学法人の支援のもとに当該第3相治験を医師主導治験として実施することの了解をえた。
現在の患者登録進捗状況(平成24年8月29日現在)は以下の如くである。
| ● | 同意取得/仮登録:25例 (内、HLAミスマッチ10例) |
| ● | 本登録:15例 |
| ● | 治験薬投与開始:15例 |
| ● | 継続中9例・中止6例 |
3.今後の方針:現在実施中(登録予定症例106例)を可及的速やかに終了させ、テーラーメイドペプチドワクチンの実用化の目途を明確にする。
参考論文:Terasaki M, Shibui S, Narita Y, Fujimaki T, Aoki T, Kajiwara K, Sawamura Y, Kurisu K, Mineta T, Yamada A, and Itoh K: Phase I Trial of a Personalized Peptide Vaccine for Patients Positive for Human Leukocyte Antigen–A24 With Recurrent or Progressive Glioblastoma Multiforme., J Clin Oncol 29:337-344. 2011,
Updating of personalized peptide vaccination to glioblastoma multiforme (GBM) patients resistant to standard therapy
1. Phase I/II study.
Long-term survival of patients with glioblastoma multiforme (GBM) remains poor even with standard combined therapy. Thus, novel therapeutic approaches are being explored, including immunotherapy. Peptide vaccination could have a bright future as a new therapeutic modality for GBM. Our phase I/II study of personalized peptide vaccination (PPV) for recurrent or progressive GBM appeared to provide a survival benefit, with median overall survival of 10.6 months (See the reference). A brief summary is as follows:
| ● | Phase 1 study: 12 patients/Extension study: 6 patients |
| ● | Recommended Dose : 3mg/1peptide |
| ● | Toxicity : All adverse events observed in Phase I study/Extension study were less than or equal to CTCAE Grade 3. There were no serious adverse vaccine-related events. |
| ● | Immunological boosting : Excellent after the 6th vaccination |
| ● | Median Vaccinations : 15.7 times |
| ● | PR : 2/12 Cases(16.7%) |
| ● | Median survival time (MST) : 10.6 months |
2. Phase III study.
Subsequently, in November 2011 we initiated a randomized double-blind phase III study of PPV for HLA-A24 positive recurrent or progressive GBM. Although randomized phase III trials are essential for commercialization, because GBM is a rare cancer with poor prognosis, these types of small, early, yet promising clinical trials are urgently needed to identify what to look for in GBM immunotherapy.
3. Future direction.
We are working as quickly as possible to demonstrate the clinical benefits of PPV in our current phase III study, as a preliminary to gaining drug approval as a therapeutic cancer vaccine.
Reference: Terasaki M, Shibui S, Narita Y, Fujimaki T, Aoki T, Kajiwara K, Sawamura Y, Kurisu K, Mineta T, Yamada A, and Itoh K: Phase I Trial of a Personalized Peptide Vaccine for Patients Positive for Human Leukocyte Antigen-A24 With Recurrent or Progressive Glioblastoma Multiforme., J Clin Oncol 29:337-344. 2011,
がんワクチン外来
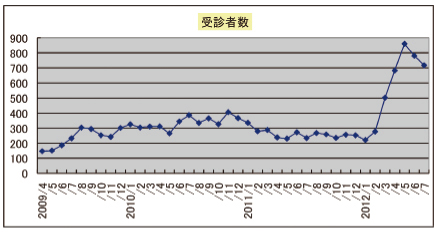
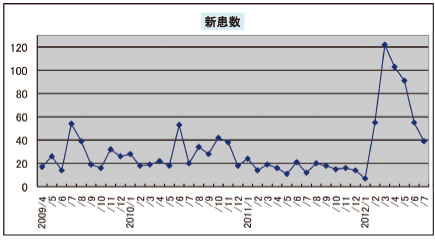
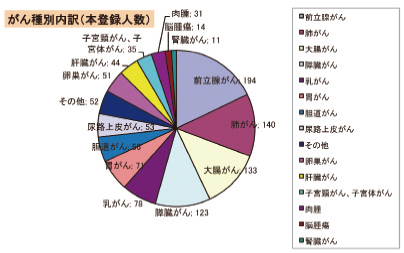
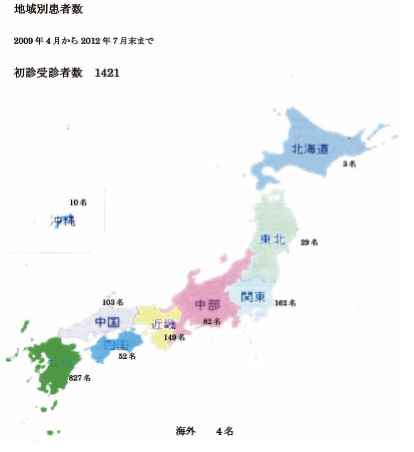
2009年4月の「がんワクチン外来」開設から3年経過し、2012年7月末までの延べ受診者数は13,365人、新患の総数は1,421人となっています。なお、2012年2月にNHKでがんワクチンに関する報道がなされて以降、受診者数が増加しました。
研究成果の一般市民への還元
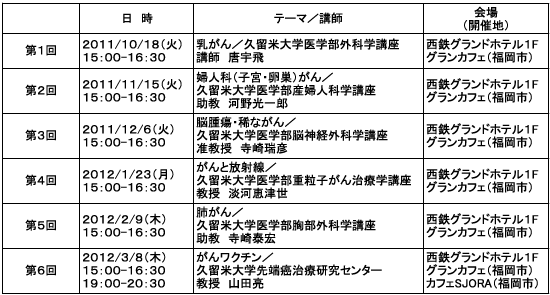
がんワクチン分子部門では、研究成果の一般市民への還元およびがんペプチドワクチン療法の普及を目的として市民公開講座を開催しています。
カフェで学ぼう がんのこと
カフェでコーヒーとケーキを食べながらリラックスした雰囲気でがんの先端医療について学んでいただく、市民公開セミナーを毎月開催しています。
NPO法人ウィッグリングジャパンと共催で、平成24年度からは福岡県「NPOと県との新たな公共サービス提案事業」として開催します。
●市民公開講座 第2回「がんを生きる」
日 時:平成23年9月3日(土) 13:00-16:00
場 所:天神イムズホール(福岡市)
テーマ:がんワクチン外来からの報告



















